Отличия дистилляции от ректификации
Дистилляция и ректификация широко используются в промышленности. Этими способами очищают этиловый спирт, из нефти выделяют керосин, бензин, ДТ и прочие компоненты, в парфюмерии получают ароматические вещества и многое другое.
В основу обеих технологий положен один и тот же принцип перегонки жидкости. Тем не менее, различия есть, и довольно серьезные.
Определение, схема устройств и принцип работы
Дистилляция
Дистилляцией называется процесс, в ходе которого жидкость, находящаяся в кубе (емкости) нагревается и испаряется, после чего охлаждается и конденсируется. Пар в итоге может переводиться в жидкость или твердое тело (второй вариант в данной статье не рассматривается). Продукт на выходе называется дистиллят. Или кубовый остаток (так называется жидкость, которая не испарилась), в зависимости от того, с какой целью перегоняли исходную смесь.
 Устройство простейшего аппарата для получения дистиллированной воды. Жидкость находится в кубе 1 с крышкой 2 и термометром 3. После нагрева емкости, вода превращается в пар, который поднимается вверх и попадает в трубку 4 с вентилем 5. А оттуда – в трубку 6, находящуюся в холодильнике 7. Чтобы пар сконденсировался и снова перешел в жидкое состояние, его надо охладить. Для этого трубка 6 омывается проточной ледяной водой. Для повышения эффективности охлаждения, она завита в спираль, чтобы пар дольше находился под действием низкой температуры. Выйдя из холодильника, жидкость попадает в сосуд для сбора дистиллята.
Устройство простейшего аппарата для получения дистиллированной воды. Жидкость находится в кубе 1 с крышкой 2 и термометром 3. После нагрева емкости, вода превращается в пар, который поднимается вверх и попадает в трубку 4 с вентилем 5. А оттуда – в трубку 6, находящуюся в холодильнике 7. Чтобы пар сконденсировался и снова перешел в жидкое состояние, его надо охладить. Для этого трубка 6 омывается проточной ледяной водой. Для повышения эффективности охлаждения, она завита в спираль, чтобы пар дольше находился под действием низкой температуры. Выйдя из холодильника, жидкость попадает в сосуд для сбора дистиллята.
При дистилляции смеси, состоящей из двух компонентов (одним из них является базовая растворяющая жидкость, а второй – в ней растворенный), в пар превращается низкокипящий, то есть тот, у которого более низкая температура кипения. А высококипящий (с более высокой температурой кипения) остается в жидком состоянии. Термометр нужен для регулирования степени нагрева так, чтобы данный параметр находился между указанными температурами.
Отличительной особенностью дистилляции является тот факт, что летучие компоненты испаряются однократно. При таком простом способе невозможно добиться высокой степени разделения составляющих смеси. Кроме того, выделяется только один ингредиент.
Ректификация
 Ректификация – это процесс, на начальном этапе которого жидкость, как и при дистилляции, тоже нагревается и испаряется. Но затем пар попадает в ректификационную колонну. В ней, за счет противотока между жидкой и газообразной фазами смеси, происходит тепловой и массовый обмен между паром и сконденсировавшимися каплями. Исходная смесь делится (притом, с высокой степенью очистки) на компоненты с разными температурами кипения за счет того, что жидкость, фактически, многократно испаряется и конденсируется.
Ректификация – это процесс, на начальном этапе которого жидкость, как и при дистилляции, тоже нагревается и испаряется. Но затем пар попадает в ректификационную колонну. В ней, за счет противотока между жидкой и газообразной фазами смеси, происходит тепловой и массовый обмен между паром и сконденсировавшимися каплями. Исходная смесь делится (притом, с высокой степенью очистки) на компоненты с разными температурами кипения за счет того, что жидкость, фактически, многократно испаряется и конденсируется.
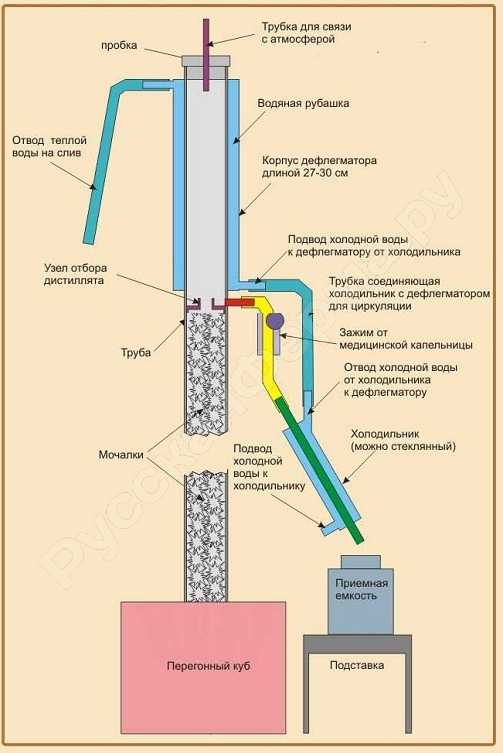
Схема простейшего ректификатора, который можно изготовить даже в домашних условиях. Он состоит из куба, подогреваемого на огне или водяной бане. Над ним расположена ректификационная колонна (в бытовых аппаратах – царга, представляющая собой жесткую трубу) с заполняющими ее насадками (на рисунке называются «мочалки», потому что для домашних устройств их нередко делают из дешевых металлических кухонных мочалок). Над ней – дефлегматор. Сбоку, напротив узла отбора дистиллята, находится специальная отводящая трубка (на схеме окрашена красным). Она соединена с холодильником и далее – с приемной емкостью. В лабораторных и бытовых ректификаторах в качестве «мочалок» применяются насадки, которыми заполняется колонна. Самые популярные: спирально призматическая (Селиваненко) и регулярно проволочная (Панченков). Первая дает самую лучшую степень очистки, вторая, при достаточно эффективной работе, наиболее простая по конструкции. Делаются, обычно, из нержавейки или меди. В промышленных установках вместо насадок применяются специальные тарелки.
 Аппарат работает следующим образом. Исходная смесь нагревается в перегонном кубе и начинает испаряться. Пар проходит через ректификационную колонну. На узле отбора дистиллята часть пара отводится через красную трубку, попадает в холодильник, конденсируется и стекает в приемную емкость. Другая часть поднимается в дефлегматор. Последний представляет собой, по сути, еще один холодильник с проточной водой в рубашке. В нем эта вторая часть пара тоже конденсируется, после чего в виде капель, которые называются флегмой или орошением, стекает в ректификационную колонну и движется внутри нее сверху вниз. Расход воды для охлаждения дефлегматора можно регулировать, тем самым изменяя количество орошения, поступающего обратно в колонну.
Аппарат работает следующим образом. Исходная смесь нагревается в перегонном кубе и начинает испаряться. Пар проходит через ректификационную колонну. На узле отбора дистиллята часть пара отводится через красную трубку, попадает в холодильник, конденсируется и стекает в приемную емкость. Другая часть поднимается в дефлегматор. Последний представляет собой, по сути, еще один холодильник с проточной водой в рубашке. В нем эта вторая часть пара тоже конденсируется, после чего в виде капель, которые называются флегмой или орошением, стекает в ректификационную колонну и движется внутри нее сверху вниз. Расход воды для охлаждения дефлегматора можно регулировать, тем самым изменяя количество орошения, поступающего обратно в колонну.
В ректификационной колонне осуществляется противоток двух фаз – пар поднимается вверх, флегма опускается вниз. Между ними происходит массовый и тепловой обмен, в результате которого пар обогащается низкокипящими (легколетучими) компонентами смеси, а капли стекающей жидкости – высококипящими (труднолетучими) ингредиентами. За счет этого, при достаточной высоте колонны, из верхней ее части (узел отбора дистиллята) выводится целевая фракция большой степени чистоты. Насадки в колонне служат для интенсификации массового и теплового обмена, поскольку конденсация пара осуществляется именно на их развитой поверхности. В промышленных установках это происходит на тарелках.
 Каждая находящаяся в колонне тарелка, называется физической (ФТ). Она нужна для того, чтобы между жидкой и паровой фазами как можно быстрее достигалось состояние равновесия. Пузырьки пара проходят сквозь находящийся на ФТ слой флегмы. В результате ускоряется массовый и тепловой обмен между фазами. Но, после прохождения пара через одну ФТ равновесия еще не будет, потому что КПД данного элемента колеблется в пределах от 50% до 60%. Таким образом, чтобы получить равновесное состояние фаз, которое бы соответствовало одной теоретической тарелке (ТТ), надо поставить две ФТ. Это значит что, если по расчету требуется колонна на 40ТТ, то в действительности в нее надо ставить 80ФТ.
Каждая находящаяся в колонне тарелка, называется физической (ФТ). Она нужна для того, чтобы между жидкой и паровой фазами как можно быстрее достигалось состояние равновесия. Пузырьки пара проходят сквозь находящийся на ФТ слой флегмы. В результате ускоряется массовый и тепловой обмен между фазами. Но, после прохождения пара через одну ФТ равновесия еще не будет, потому что КПД данного элемента колеблется в пределах от 50% до 60%. Таким образом, чтобы получить равновесное состояние фаз, которое бы соответствовало одной теоретической тарелке (ТТ), надо поставить две ФТ. Это значит что, если по расчету требуется колонна на 40ТТ, то в действительности в нее надо ставить 80ФТ.
Установки для ректификации бывают непрерывные и периодические.
В первых жидкая смесь все время подается в колонну, и также постоянно из нее выводятся разделенные ингредиенты. Во вторых в куб сразу загружается определенное количество смеси, после чего аппарат работает до полной ее переработки.
В бытовых устройствах в качестве ректификационной колонны используется царга. Это труба диаметром от 30мм до 50мм, заполненная по всему объему насадками. Чтобы последние не высыпались, по краям ставят проницаемые для пара и капель пыжи. Состояние равновесия фаз достигается в том случае, когда пар проходит через некоторый слой царги, эквивалентный одной ТТ. Его высоту рассчитывают в миллиметрах и называют высотой единицы переноса.
Главные особенности ректификации: выделение нужного ингредиента в чистом виде и возможность разделения исходной смеси сразу на несколько компонентов. Чем выше колонна, тем медленнее идет процесс, но тем чище конечный продукт.
Процессы в виноделии
В отрасли изготовления алкогольных напитков, разница между дистиллированным и ректифицированным спиртом объясняется следующим образом. Дистиллят – это сырье, в котором остается органолептика (вкус и запах) исходного продукта. То есть, если делается напиток зерновой, то зерна, если яблочный – яблока и так далее. При этом в дистиллированном этиловом спирте еще есть множество примесей. Часть из них формируют вкус и запах. От прочих избавляются с помощью различных рецептов. Ректификат – это рафинированно очищенный спирт. Органолептика исходного продукта полностью отсутствует. В нем вкус и запах только спирта, и больше – ничего. На следующих стадиях технологического процесса, с помощью вкусовых добавок и ароматизаторов, в него вносят заданную органолептику, после чего получают широкий ассортимент наливок, настоек и прочего.
Исходя из этого, нельзя говорить, что один способ лучше, а другой – хуже. У каждого свое предназначение. Если, например, делается бренди со вкусом и ароматом винограда, то нужна дистилляция. После ректификации указанные особенности исчезнут. Для получения приятного аромата, дистиллированный спирт выдерживают в дубовых бочках. А для ректифицированного 96%-го спирта это бесполезно, он годится лишь для разведения, например, при изготовлении водки. К этому еще можно добавить, что оборудование для ректификации спирта стоит дороже, чем для дистилляции. К тому же, для проведения ректификации требуется дистиллированная брага.
Теоретические основы дистилляции
В смеси, состоящей из двух ингредиентов (одним из которых является жидкость, как основа раствора), концентрация растворенного вещества в жидкости С1 отличается от концентрации С2 его же в паре этой жидкости. Коэффициент разделения (распределения)
В = С2 / С1
является характеристикой процесса. В некоторых случаях удобней работать с обратной величиной: А = 1 / В, которая называется так же. Данный параметр зависит от условий проведения дистилляции и природы веществ, составляющих смесь.
В зависимости от условий, коэффициент В может быть:
-
Идеальный. На него влияют только парциальные давления ингредиентов смеси (парциальным называется давление отдельно взятого газа, входящего в смесь из нескольких газов; то есть, это давление одного газа, которое у него было бы, если бы он занимал весь объем, который занимает смесь газов).
-
Равновесный. В этом случае число молекул газа Н, улетучивающихся из жидкости, равно числу его молекул Н1, которые возвращаются в жидкость за то же время.
-
Эффективный.
На практике на проведение дистилляции влияют перемешивание раствора и наличие в нем примесей. Присутствие последних может оказаться настолько значительным, что по разделению основного вещества и примесей эффективный коэффициент может очень сильно отличаться от идеального.
Не менее важными параметрами процесса являются температура испарения и степень отклонения системы от фазового равновесия между жидкостью и паром. Во время дистилляции:
Н = Н1 + НС
Где НС – число молекул, переходящих в конденсат. Количественно отклонение определяется соотношением: НС / Н. В этом случае есть два предельных состояния системы. Если НС = 0, то имеет место равновесие, сколько частиц ушло из жидкости за единицу времени, столько же в нее и вернулось. Если НС = Н, то это молекулярная дистилляция, то есть, все частицы, испарившиеся из жидкости, перешли в конденсат. Обычно такое бывает, если процесс проводится в вакууме, давление пара небольшое, а расстояние от поверхности воды до точки конденсации минимальное. В этом случае частицы пара не сталкиваются, ни с молекулами воздуха, ни между собой.
Виды дистилляции
Описанный в начале статьи процесс, при котором жидкость нагревается и частично испаряется, а ее пары непрерывно отводятся в холодильник и там конденсируются, называется простой перегонкой. При работе с многокомпонентной жидкой смесью, применяется дробная перегонка или фракционная дистилляция. В этом случае ингредиенты смеси собирают в конденсат по частям, в зависимости от их летучести, начиная с самого низкокипящего.
Ректификация многими специалистами считается разновидностью дистилляции. Она происходит за счет того, что любая замкнутая система, состоящая из газа и жидкости, стремится к состоянию равновесия. А при ректификации рабочая (фактическая) концентрация ингредиентов паровой фазы отличается от той, которая должна быть, чтобы данная жидкость находилась в равновесии.
Дистилляция и ректификация – это два способа разделения компонентов жидкой смеси, в основе которых лежит один и тот же физический процесс. Но разные технологии их проведения позволяют получить на выходе совершенно различные результаты.
www.russkayaferma.ru
Что такое дистилляция самогона и как ее правильно проводить
В своих уроках я часто употребляю термин «дистилляция» или «дистилляты». Что это за технология, в чем ее особенности и секреты? Сегодня вы узнаете все о классической технологии дистилляции. Звонок прозвенел – начинаем урок.

Термин дистилляция означает «стекание каплями»
Что такое классическая дистилляция
Термин имеет латинское происхождение, в дословном переводе означает «стекание каплями».
Суть процесса состоит в разделении спиртосодержащей смеси на различные фракции.
Механизм процесса основывается на разнице температур испарения различных жидкостей. Мы из школьного курса знаем, что вода испаряется при 100 оС, а спирт – при 78,4 оС. Спиртосодержащая смесь – брага – в перегонном кубе подвергается нагреву в определенных температурных диапазонах. В результате часть фракций испаряется. Пар попадает в холодильник, где охлаждается и конденсируется, переходя в жидкое состояние. Дистилляция происходит постепенно, и конденсат стекает в емкость буквально по каплям. Отсюда и латинское название процесса – «distillatio».
Для дистилляции есть и русскоязычный термин – «перегонка». Это название тоже прекрасно передает суть процесса.

Тихо! Идет дистилляция!
Зачем нам дистилляция?
Перебродившее сусло не является готовым к употреблению напитком. В его составе от 10 до 20 % спирта, от 90 до 80 % воды и множество самых разных химических веществ, в том числе ацетоны, уксусные альдегиды и другие элементы, которые очень вредят организму. Дистилляция выполняет двойную функцию:
- Повышает крепость конечного продукта путем отделения части воды и сохранения количества спирта в готовом продукте.
- Очищает его от вредных примесей, позволяя выделить и отбросить наиболее опасные фракции.
Дистилляция: первый этап
Итак, брага у нас готова, оборудование для перегонки мы выбрали. Пора начинать дистилляцию.
Температура в перегонном кубе во время дистилляции поддерживается на промежуточном уровне между показателями кипения спирта и воды. То есть ниже, чем 100 градусов, но выше, чем 78,4. Для зерновых браг вполне достаточной будет температура 83–84 градуса по Цельсию. А в общем случае температурный режим рассчитывается исходя из содержания спирта в браге.
Пар поступает в охлаждающую камеру, конденсируется на холодной поверхности и капли стекают в резервуар. Первая партия продукта будет иметь содержание спиртов выше, а последняя – ниже. Происходит это по причине постепенного испарения не только спиртовой, но и водной фракции.
В результате первичной перегонки получаем спирт-сырец крепостью до 45 %. В нем все еще содержатся вредные веществ
cosmogon.ru
Дистилляция — это… Что такое Дистилляция?
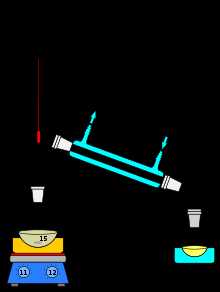 Устройство простейшего перегонного аппарата.
Устройство простейшего перегонного аппарата.1 Нагревательный элемент
2 Перегонный куб
3 Отводная трубка или насадка Вюрца
4 Термометр
5 Холодильник
6 Подвод охлаждающей жидкости
7 Отвод охлаждающей жидкости
8 Приёмная колба
9 Отвод газа (в том числе с понижением давления)
10 Аллонж
11 Регулятор температуры нагревателя
12 Регулятор скорости перемешивания
13 Магнитная мешалка
14 Водяная (масляная, песочная и т. п.) баня
15 Мешалка или «кипелки»
16 Охлаждающая ванна
Дистилляция (лат. distillatio — стекание каплями) — перегонка, испарение жидкости с последующим охлаждением и конденсацией паров. Различают дистилляцию с конденсацией пара в жидкость (при которой получаемый конденсат имеет усреднённый состав вследствие перемешивания) и дистилляцию с конденсацией пара в твёрдую фазу (при которой в конденсате возникает распределение концентрации компонентов). Продуктом дистилляции является конденсат или остаток (или и то, и другое) – в зависимости от дистиллируемого вещества и целей процесса. Основными деталями дистилляционного устройства являются обогреваемый контейнер (куб) для дистиллируемой жидкости, охлаждаемый конденсатор (холодильник) и соединяющий их обогреваемый паропровод.
История
До X века, у Авиценны дистилляция упоминается как метод получения эфирных масел.
Применение
Дистилляция применяется в промышленности и в лабораторной практике для разделения и рафинирования сложных веществ: для разделения смесей органических веществ (например, разделение нефти на бензин, керосин, соляр и др.; получение ароматических веществ в парфюмерии; получение алкогольного спирта) и для получения высокочистых неорганических веществ (например, металлов: бериллий, цинк, магний, кадмий и др.).
Теория
В теории дистилляции в первую очередь рассматриваются двухкомпонентные вещества. Действие дистилляции основано на том, что концентрация некоторого компонента в жидкости отличается от его концентрации в паре, образующемся из этой жидкости. Отношение = является характеристикой процесса и называется коэффициентом разделения при дистилляции. Коэффициент разделения зависит от природы разделяемых компонентов и режима дистилляции.
Режимы дистилляции характеризуются температурой испарения и степенью отклонения от фазового равновесия жидкость-пар. Обычно в дистилляционном процессе n=+, где n — число частиц вещества, переходящих в единицу времени из жидкости в пар, — число частиц, возвращающихся в это же время из пара в жидкость, — число частиц, переходящих в это время в конденсат. Отношение /n является показателем отклонения процесса от равновесного. Предельными являются режимы, в которых =0 (равновесное состояние системы жидкость-пар) и =n (режим молекулярной дистилляции).
При =0, когда число частиц, покидающих в единицу времени жидкость, равно числу частиц, возвращающихся в это же время в жидкость, равновесный коэффициент разделения двухкомпонентного вещества может быть выражен через давления и чистых компонентов при температуре процесса: , где и — так называемые коэффициенты активности, учитывающие взаимодействие компонентов в жидкости. Эти коэффициенты имеют температурную и концентрационную зависимости (см. активность (химия)). С понижением температуры значение коэффициента разделения обычно удаляется от единицы, т. е. эффективность разделения при этом увеличивается.
При =n все испаряющиеся частицы переходят в конденсат (режим молекулярной дистилляции). В этом режиме коэффициент разделения , где и — молекулярные массы первого и второго компонентов соответственно. Режим молекулярной дистилляции может применяться в различных дистилляционных способах, включая ректификацию. Обычно молекулярная дистилляция осуществляется в вакууме при низком давлении пара и при близком расположении поверхности конденсации к поверхности испарения (что исключает столкновение частиц пара друг с другом и с частицами атмосферы). В режиме, близком к молекулярной дистилляции, проводится дистилляция металлов. В связи с тем, что коэффициент разделения при молекулярной дистилляции зависит не только от парциальных давлений компонентов, но и от их молекулярных (или атомных) масс, молекулярная дистилляция может применяться для разделения смесей, для которых , — азеотропных смесей, включая смеси изотопов.
Для различных режимов дистилляции выведены уравнения, связывающие содержание второго компонента в конденсате и в остатке с долей перегонки или с долей остатка при заданных условиях процесса и известной начальной концентрации жидкости (, и — масса конденсата и остатка, а также начальная масса дистиллируемого вещества соответственно). Расчёты проводятся в предположении идеального перемешивания дистиллируемой жидкости, а также жидкого конденсата. Также выведены уравнения распределения компонентов в твёрдом конденсате, получаемого дистилляцией с направленным затвердеванием конденсата или зонной дистилляцией. Параметром этих уравнений является коэффициент разделения α для заданных условий дистилляции.
При дистилляции вещества с большой концентрацией компонентов с конденсацией пара в жидкость при несильной зависимости коэффициентов активности компонентов от их концентраций взаимосвязь величин , и , когда используются концентрации в процентах, имеет вид:
.
Для дистилляции с конденсацией пара в жидкость при малом содержании примеси
,
=.
Дистилляционные уравнения могут использоваться для описания процессов распределения примесей в других фазовых переходах из фазы с интенсивным перемешиванием (таких как переходы жидкий кристалл-кристалл, жидкий кристалл-жидкость, газ-плазма, а также в переходах, связанных с квантово-механическими состояниями – сверхтекучая жидкость, конденсат Бозе-Эйнштейна) – при подстановке в них соответствующих коэффициентов распределения.
Дистилляция с конденсацией пара в жидкость (простая перегонка, фракционная дистилляция, ректификация)
Простая перегонка — частичное испарение жидкой смеси путём непрерывного отвода и конденсации образовавшихся паров в холодильнике. Полученный конденсат называется дистиллятом, а неиспарившаяся жидкость — кубовым остатком.
Фракционная дистилляция (или дробная перегонка) — разделение многокомпонентных жидких смесей на отличающиеся по составу части — фракции путём сбора конденсата частями с различной летучестью, начиная с первой, обогащенной низкокипящим компонентом. Остаток жидкости обогащён высококипящим компонентом. Для улучшения разделения фракций применяют дефлегматор.
Ректификация — способ дистилляции, при котором часть жидкого конденсата (флегма) постоянно возвращается в куб, двигаясь навстречу пару в контакте с ним. В результате этого примеси, содержащиеся в паре, частично переходят во флегму и возвращаются в куб, при этом чистота пара (и конденсата) повышается (См. ректификация, ректификационная колонна).
Дистилляция с конденсацией пара в твёрдую фазу (с конденсацией пара в градиенте температуры; с направленным затвердеванием конденсата; зонная дистилляция)
Дистилляция с конденсацией пара в градиенте температуры – дистилляционный процесс, в котором конденсация в твёрдую фазу осуществляется на поверхности, имеющей градиент температуры, с многократным реиспарением частиц пара. Менее летучие компоненты осаждаются при более высоких температурах. В результате в конденсате возникает распределение примесей вдоль температурного градиента, и наиболее чистая часть конденсата может быть выделена в качестве продукта. Разделение компонентов пара при реиспарении подчиняется собственным закономерностям. Так, при молекулярной дистиляции соотношение между количествами и осаждённых в конденсаторе первого и второго компонентов, соответственно, выражается равенством:
,
где и — скорости испарения первого компонента из расплава и с поверхности реиспарения соответственно, и — то же для второго компонента, и — коэффициенты конденсации первого и второго компонентов соответственно, μ – коэффициент, зависящий от поверхности испарения и углов испарения и реиспарения. Реиспарение повышает эффективность очистки от трудноудаляемых малолетучих примесей в 2-5 раз, а от легколетучих — на порядок и более (по сравнению с простой перегонкой). Этот вид дистилляции нашёл применение в промышленном производстве высокочистого бериллия.
Дистилляция с направленным затвердеванием конденсата (дистилляция с вытягиванием дистиллята) – дистилляционный процесс в контейнере удлинённой формы c полным расплавлением дистиллируемого вещества и конденсацией пара в твёрдую фазу по мере вытягивания конденсата в холодную область. Процесс разработан теоретически.
В получаемом конденсате возникает неравномерное распределение примесей, и наиболее чистая часть конденсата может быть выделена в качестве продукта. Процесс является дистилляционным аналогом нормальной направленной кристаллизации. Распределение примеси в конденсате описывается уравнением:
,
где С – концентрация примеси в дистилляте на расстоянии х от начала, L – высота конденсата при полностью испарившемся дистиллируемом материале.
Зонная дистилляция — дистилляционный процесс в контейнере удлинённой формы c частичным расплавлением рафинируемого вещества в перемещаемой жидкой зоне и конденсацией пара в твёрдую фазу по мере выхода конденсата в холодную область. Процесс разработан теоретически.
При движении зонного нагревателя вдоль контейнера сверху вниз в контейнере формируется твёрдый конденсат с неравномерным распределением примесей, и наиболее чистая часть конденсата может быть выделена в качестве продукта. Процесс может быть повторён многократно, для чего конденсат, полученный в предыдущем процессе, должен быть перемещён (без переворота) в нижнюю часть контейнера на место рафинируемого вещества. Неравномерность распределения примесей в конденсате (т. е. эффективность очистки) растёт с увеличением числа повторений процесса.
Зонная дистилляция является дистилляционным аналогом зонной перекристаллизации. Распределение примесей в конденсате описывается известными уравнениями зонной перекристаллизации с заданным числом проходов зоны – при замене коэффициента распределения k для кристаллизации на коэффициент разделения α для дистилляции. Так, после одного прохода зоны
,
где С – концентрация примеси в конденсате на расстоянии х от начала конденсата, λ – длина жидкой зоны.
См. также
Литература
- Девятых Г.Г., Еллиев Ю.Е. Введение в теорию глубокой очистки веществ. — М.: Наука, 1981. — 320 с.
- Девятых Г.Г., Еллиев Ю.Е. Глубокая очистка веществ. — М.: Высшая школа, 1974. — 180 с.
- Степин Б.Д., Горштейн И.Г., Блюм Г.З., Курдюмов Г.М., Оглоблина И.П. Методы получения особо чистых неорганических веществ. — Л.: Химия, 1969. — 480 с.
- Корякин Ю.В., Ангелов И.И. Чистые химические вещества. Руководство по приготовлению неорганических реактивов и препаратов в лабораторных условиях. — М.: Химия, 1974. — с.
- Беляев А.И. Физико-химические основы очиски металлов и полупроводниковых веществ. — М.: Металлургия, 1973. — 320 с.
- Пазухин В.А., Фишер А.Я. Разделение и рафинирование металлов в вакууме. — М.: Металлургия, 1969. — 204 с.
- Иванов В.Е., Папиров И.И., Тихинский Г.Ф., Амоненко В.М. Чистые и сверхчистые металлы (получение методом дистилляции в вакууме). — М.: Металлургия, 1965. — 263 с.
- Несмеянов А.Н. Давление пара химических элементов. — М.: Издательство АН СССР, 1961 — 320 с.
- Кравченко А.И. О временной зависимости состава двойного сплава при его разгонке в вакууме // Известия АН СССР. Серия: Металлы. — 1983. — № 3. — С. 61-63.
- Кравченко А.И. Об уравнениях дистилляции при малом содержании примеси // Вопросы атомной науки и техники, 1990. — № 1 — Серия: «Ядерно-физические исследования» (9). — С. 29-30.
- Нисельсон Л.Я., Ярошевский А.Г. Межфазовые коэффициенты распределения (Равновесия кристалл-жидкость и жидкость-пар). — М.: Наука, 1992. — 399 с.
- Kravchenko A.I. Simple substances refining: efficiency of distillation methods // Functional Materials, 2000 — V.7. — N. 2. — P. 315-318.
- Кравченко А.И. Уравнение распределения примеси в твёрдом дистилляте // Неорганические материалы, 2007. — Т. 43. — № 8. — С. 1021-1022.
- Кравченко А.И. Эффективность очистки в дистилляционном и кристаллизационном процессах // Неорганические материалы, 2010. — Т. 46. — № 1. — С. 99-101.
- Кравченко А.И. Дистилляция с вытягиванием дистиллята // Вопросы атомной науки и техники, 2008. — № 1 — Серия: «Вакуум, чистые материалы, сверхпроводники» (17). — С. 18-19. [1]
- Кравченко А.И. Зонная дистилляция // Вопросы атомной науки и техники, 2011. — № 6 — Серия: «Вакуум, чистые материалы, сверхпроводники» (19). — С. 24-26. [2]
- Кравченко А.И. О распределении примесей при фазовых переходах из фазы с идеальным перемешиванием // Вопросы атомной науки и техники, 2011. — № 6 — Серия: «Вакуум, чистые материалы, сверхпроводники» (19). — С. 27-29. [3]
- ГОСТ 2177 (ASTM D86)
Галерея
dic.academic.ru
Дистилляция — это… Что такое Дистилляция?
перегонка, разделение жидких смесей на отличающиеся по составу фракции. Процесс основан на различии температур кипения компонентов смеси. В зависимости от физических свойств компонентов разделяемых жидких смесей применяют различные способы Д.
Простая Д. (рис. 1) проводится частичным испарением кипящей жидкой смеси, непрерывным отводом и последующей конденсацией образовавшихся паров. Так как пары над кипящей жидкой смесью содержат низкокипящих компонентов больше, чем жидкость, то конденсат (называемый дистиллятом) обогащается, а неиспарившаяся жидкость (кубовый остаток) обедняется ими. В дистилляционном кубе 1 кипит исходная жидкая смесь. Образующиеся пары непрерывно отводятся в конденсатор 2, где образуется дистиллят, который стекает в приёмник 3. При простой Д. содержание низкокипящих компонентов в паровой и жидкой фазах непрерывно падает. Поэтому состав дистиллята меняется во времени. Простая Д., осуществляемая по описанной схеме, — периодический процесс. Для ускорения процесса применяют полунепрерывную Д., при которой в дистилляционный куб непрерывно поступает исходная смесь, равная массе уходящих паров.
Фракционная Д., называемая также дробной перегонкой (рис. 2), — одна из разновидностей простой Д. Такую Д. применяют для разделения смеси жидкостей на фракции, кипящие в узких интервалах температур. При этом дистилляты разных составов отводят (последовательно во времени) в несколько сборников. В сборник 1 поступает первая по времени порция дистиллята, наиболее богатая низкокипящими компонентами, в сборник 2 — менее богатая, в сборник 3 — ещё менее богатая и т.д. В каждом из этих дистиллятов (фракциях) преобладает один или несколько компонентов исходной смеси с близкими температурами кипения. Простую Д. для улучшения разделения смесей часто комбинируют с противоточной дефлегмацией (рис. 3). При этом образующиеся в кубе 1 пары частично конденсируются в дефлегматоре 2, конденсат (флегма) непрерывно возвращается в куб, а остаток паров после дефлегматора поступает в конденсатор 3, откуда дистиллят стекает в сборник 4. Этим способом достигается большее обогащение дистиллята низкокипящими компонентами, т.к. при частичной конденсации (дефлегмации) паров преимущественно конденсируются высококипящие компоненты.
Равновесная Д. (однократное испарение) характеризуется испарением части жидкости и продолжительным контактом паров с неиспарившейся жидкостью до достижения фазового равновесия (рис. 4). Разделяемая смесь проходит по трубам 1, обогреваемым снаружи топочными газами. Образовавшаяся при этом парожидкостная смесь, близкая к равновесному состоянию, поступает в сепаратор 2 для механического отделения жидкости от пара. Пары (П) из сепаратора поступают в конденсатор, откуда дистиллят стекает в приёмник, а оставшаяся в сепараторе жидкость отводится в сборник. В этом процессе соотношение между паром и жидкостью определяется материальным балансом и условиями фазового равновесия. Равновесная Д. редко применяется для двухкомпонентных смесей; хорошие результаты получают в основном в случае многокомпонентных смесей, из которых можно получить фракции, сильно различающиеся по составу.
Д. в токе водяного пара или инертных газов применяют, когда необходимо понизить температуру процесса отгонки, в случае разделения нетермостойких компонентов, а также для отгонки веществ с низкой температурой испарения от компонентов с высокой температурой испарения. Пузырьки водяного пара или инертного газа барботируют через слой жидкости (см. Барботирование). При Д. с водяным паром образовавшаяся смесь паров воды и летучего компонента отводится из аппарата и подвергается конденсации и охлаждению. Состав образующихся в кубе паров не зависит от состава жидкости, а температура кипения смеси всегда ниже температуры кипения каждого из компонентов при данном давлении. При Д. с инертным газом компоненты раствора испаряются в поток газа, даже если раствор не кипит, а парообразование при испарении может происходить при любых температурах, вне зависимости от внешнего давления, что позволяет вести процесс при низких температурах.Молекулярная Д. основана на разделении жидких смесей свободным их испарением в высоком вакууме 133—13,3 мн/м2 (10-3—10-4мм рт. ст.) при температуре ниже точки их кипения. Процесс проводят при взаимном расположении поверхностей испарения и конденсации на расстоянии, меньшем длины свободного пробега молекул перегоняемого вещества. Благодаря вакууму молекулы пара движутся от испаряющей поверхности к конденсирующей с минимальным числом столкновений. При молекулярной Д. изменение состава пара по сравнению с составом жидкости определяется различием скоростей испарения компонентов. Поэтому этим способом можно разделять смеси, компоненты которых обладают одинаковым давлением паров. При данной температуре жидкости и соответствующем ей давлении паров скорость молекулярной Д. растёт с понижением давления в аппарате.
Для уменьшения времени диффузии молекул летучего компонента из глубины слоя жидкости к поверхности испарения процесс в современных молекулярных кубах проводят в очень тонких плёнках жидкости, что позволяет, кроме того, уменьшить время нахождения вещества на поверхности испарения и опасность его термического разложения. Для молекулярной Д. применяют аппараты с горизонтальными и вертикальными поверхностями испарения, а также получившие наибольшее промышленное применение центробежные аппараты. В последних процесс характеризуется наименьшими толщиной жидкой плёнки (в среднем 0,05 мм) и временем её пребывания на поверхности нагрева (0,03—1,2 сек). В центробежных аппаратах (рис. 5) на испаритель 1, представляющий собой быстровращающийся конус (иногда диск), подаётся разделяемая смесь. Центробежная сила перемещает жидкость от центра к периферии (вверх). Пары перегоняемого вещества собираются на неподвижном конденсаторе 2, расположенном параллельно поверхности испарителя, откуда дистиллят непрерывно отводится. Остаток после перегонки сбрасывается в кольцевой жёлоб 3 и выводится из куба. Для увеличения эффекта разделения устанавливают несколько аппаратов последовательно.
Молекулярную Д. применяют для разделения и очистки высокомолекулярных и термически нестойких органических веществ, например для очистки эфиров себациновой, стеариновой, олеиновой и др. кислот, для выделения витаминов из рыбьего жира и различных растительных масел, при производстве медицинских препаратов, вакуумных масел и др.
В металлургии понятие Д. объединяет пирометаллургические процессы (см. Пирометаллургия), основанные на переводе восстанавливаемого металла (см. Восстановление металлов) в парообразное состояние с последующей конденсацией. Металлургическая Д. — сочетание химического (окислительно-восстановительной реакции) и физического (испарения и конденсации) процессов. Восстановление проводят с использованием углеродистых восстановителей (см. Карботермия) или металлотермическим способом (см. Металлотермия). Возможно выделение свободного металла при окислительном обжиге сульфидных концентратов. Степень разделения при Д. определяется различием состава перегоняемой смеси и её пара. Полнота перехода металла в газовую фазу при Д. определяется восстановлением металлов при температурах и давлениях, обеспечивающих получение восстановленного металла в парообразном агрегатном состоянии.Лит.: Касаткин А. Г., Основные процессы и аппараты химической технологии, 8 изд., М., 1971; Гельперин Н. И., Дистилляция и ректификация, М. — Л., 1947; Багатуров С. А., Теория и расчет перегонки и ректификации, М., 1961; Циборовский Я., Процессы химической технологии, пер. с польск., Л., 1958; Матрозов В. И., Аппаратура для молекулярной дистилляции, М., 1954; Чижиков Д. М., Металлургия тяжелых цветных металлов, М. — Л., 1948; Лакерник М. М., Электротермия в металлургии меди, свинца и цинка, М., 1964.
В. Л. Пебалк.
Рис. 1 к ст. Дистилляция.
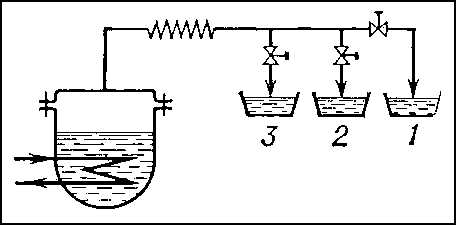
Рис. 2 к ст. Дистилляция.
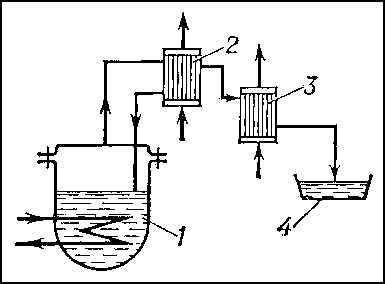
Рис. 3 к ст. Дистилляция.

Рис. 4 к ст. Дистилляция.
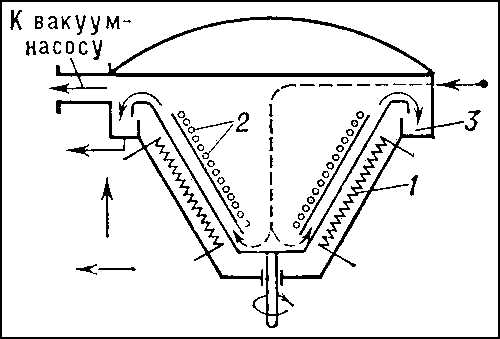
Рис. 5 к ст. Дистилляция.
dic.academic.ru
Дистилляция — это… Что такое Дистилляция?
Дистилляция
Дистилляция (от лат. distillatio – стекание каплями) – перегонка, разделение жидких смесей на отличающиеся по составу фракции. Процесс основан на различии температур кипения компонентов смеси.
Процесс дистилляции был известен в Древнем Китае и Риме во втором тысячелетии до нашей эры и применялся главным образом для выделения душистых веществ из ароматических растений. Египтяне, постигнув тайны дистилляции вина, изобрели перегонный аппарат (аламбик), получивший впоследствии большое распространение у других народов.
Описание способа дистилляции и его использования в лечебных целях приводится в трудах персидского ученого Авиценны (930–1037).
В Древней Руси упоминание о постройке винокурни для получения «хлебного вина» водки относится к 1174 году.
Определенная роль в совершенствовании процесса дистилляции принадлежит алхимикам средневековья, но наибольшее развитие она получила в конце 19 – начале 20 веков в связи с внедрением в промышленности (спиртовой, нефтеперерабатывающей и др.) высокопроизводительных колонных аппаратов.
В зависимости от физических свойств компонентов разделяемых жидких смесей применяют различные способы дистилляции.
Простая дистилляция проводится частичным испарением кипящей жидкой смеси, непрерывным отводом и последующей конденсацией образовавшихся паров. Так как пары над кипящей жидкой смесью содержат низкокипящих компонентов больше, чем жидкость, то конденсат (называемый дистиллятом) обогащается, а неиспарившаяся жидкость (кубовый остаток) обедняется ими. При простой дистилляции содержание низкокипящих компонентов в паровой и жидкой фазах непрерывно падает. Поэтому состав дистиллята меняется во времени. Простая дистилляция – периодический процесс. Для ускорения процесса применяют полунепрерывную дистилляцию, при которой в дистилляционный куб непрерывно поступает исходная смесь, равная массе уходящих паров.
Фракционная дистилляция, называемая также дробной перегонкой, – одна из разновидностей простой дистилляции. Такую дистилляцию применяют для разделения смеси жидкостей на фракции, кипящие в узких интервалах температур. При этом дистилляты разных составов отводят (последовательно во времени) в несколько сборников. В каждом из этих дистиллятов (фракциях) преобладает один или несколько компонентов исходной смеси с близкими температурами кипения. Простую дистилляцию для улучшения разделения смесей часто комбинируют с противоточной дефлегмацией (частичная конденсация). При этом образующиеся в кубе пары частично конденсируются в дефлегматоре, конденсат (флегма) непрерывно возвращается в куб, а остаток паров после дефлегматора поступает в конденсатор, откуда дистиллят стекает в сборник. Этим способом достигается большее обогащение дистиллята низкокипящими компонентами, т.к. при дефлегмации паров преимущественно конденсируются высококипящие компоненты.
Равновесная дистилляция (однократное испарение) характеризуется испарением части жидкости и продолжительным контактом паров с неиспарившейся жидкостью до достижения фазового равновесия. Разделяемая смесь проходит по трубам, обогреваемым снаружи топочными газами. Образовавшаяся при этом парожидкостная смесь, близкая к равновесному состоянию, поступает в сепаратор для механического отделения жидкости от пара. Пары из сепаратора поступают в конденсатор, откуда дистиллят стекает в приемник, а оставшаяся в сепараторе жидкость отводится в сборник. В этом процессе соотношение между паром и жидкостью определяется материальным балансом и условиями фазового равновесия. Равновесная дистилляция редко применяется для двухкомпонентных смесей; хорошие результаты получают в основном в случае многокомпонентных смесей, из которых можно получить фракции, сильно различающиеся по составу.
Дистилляцию в токе водяного пара или инертных газов применяют, когда необходимо понизить температуру процесса отгонки, в случае разделения нетермостойких компонентов, а также для отгонки веществ с низкой температурой испарения от компонентов с высокой температурой испарения. Пузырьки водяного пара или инертного газа барботируют (продавливают) через слой жидкости. При дистилляции с водяным паром образовавшаяся смесь паров воды и летучего компонента отводится из аппарата и подвергается конденсации и охлаждению. Состав образующихся в кубе паров не зависит от состава жидкости, а температура кипения смеси всегда ниже температуры кипения каждого из компонентов при данном давлении. При дистилляции с инертным газом компоненты раствора испаряются в поток газа, даже если раствор не кипит, а парообразование при испарении может происходить при любых температурах, вне зависимости от внешнего давления, что позволяет вести процесс при низких температурах.
Молекулярная дистилляция основана на разделении жидких смесей свободным их испарением в высоком вакууме 133–13,3 мн/м2 (10–3–10–4 мм ртутного столба) при температуре ниже точки их кипения. Процесс проводят при взаимном расположении поверхностей испарения и конденсации на расстоянии, меньшем длины свободного пробега молекул перегоняемого вещества. Благодаря вакууму молекулы пара движутся от испаряющей поверхности к конденсирующей с минимальным числом столкновений. При молекулярной дистилляции изменение состава пара по сравнению с составом жидкости определяется различием скоростей испарения компонентов. Поэтому этим способом можно разделять смеси, компоненты которых обладают одинаковым давлением паров. При данной температуре жидкости и соответствующем ей давлении паров скорость молекулярной дистилляции растет с понижением давления в аппарате.
Для молекулярной дистилляции применяют аппараты с горизонтальными и вертикальными поверхностями испарения, а также получившие наибольшее промышленное применение центробежные аппараты. В последних процесс характеризуется наименьшими толщиной жидкой пленки (в среднем 0,05 мм) и временем ее пребывания на поверхности нагрева (0,03м–1,2 сек). В центробежных аппаратах на испаритель, представляющий собой быстровращающийся конус (иногда диск), подается разделяемая смесь. Центробежная сила перемещает жидкость от центра к периферии (вверх). Пары перегоняемого вещества собираются на неподвижном конденсаторе, расположенном параллельно поверхности испарителя, откуда дистиллят непрерывно отводится. Остаток после перегонки сбрасывается в кольцевой желоб и выводится из куба. Для увеличения эффекта разделения устанавливают несколько аппаратов последовательно.
Молекулярную дистилляцию применяют для разделения и очистки высокомолекулярных и термически нестойких органических веществ, например для очистки эфиров себациновой, стеариновой, олеиновой и других кислот, для выделения витаминов из рыбьего жира и различных растительных масел, при производстве медицинских препаратов, вакуумных масел и др.
В металлургии понятие дистилляции объединяет пирометаллургические процессы, основанные на переводе восстанавливаемого металла в парообразное состояние с последующей конденсацией. Металлургическая дистилляция – сочетание химического (окислительно-восстановительной реакции) и физического (испарения и конденсации) процессов. Восстановление проводят с использованием углеродистых восстановителей или металлотермическим способом. Возможно выделение свободного металла при окислительном обжиге сульфидных концентратов. Степень разделения при дистилляции определяется различием состава перегоняемой смеси и ее пара. Полнота перехода металла в газовую фазу при дистилляции определяется восстановлением металлов при температурах и давлениях, обеспечивающих получение восстановленного металла в парообразном агрегатном состоянии.
Дистилляция применяется также в химической, лесохимической, фармацевтической и других отраслях промышленности для грубого разделения смесей на фракции, когда не предъявляются высокие требования к чистоте получаемых продуктов, а также для очистки жидких смесей от нелетучих или малолетучих примесей.
Дистилляцию с дефлегмацией применяют в нефтепереработке и лабораторной практике, дистилляция с водяным паром – в химической, нефтехимической, парфюмерной и других отраслях промышленности для отгонки высококипящих компонентов из вязких смесей, содержащих значительные количества твердых или малолетучих жидких веществ. Также путем перегонки (однократной или многократной) на ликеро-водочных заводах получают полуфабрикат для множества алкогольных напитков: коньяка, рома, виски, а в домашних условиях – самогон.
В лабораторной практике условия дистилляции для некоторых видов продуктов стандартизованы. Наиболее известными являются ГОСТ 2177(ASTM D86) – перегонка 100 мл продукта с температурой кипения от комнатной до 400°С при атмосферном давлении. Это сделано для воспроизводимости результатов тестирования бензина, керосина, дизельного топлива, нефти, а также различных растворителей.
Дистилляция является давно известным и проверенным способом глубокой очистки воды.
Хорошо всем известный пример использования дистиллированной воды – заливка в аккумуляторы автомобиля. В быту же дистилляторы не нашли широкого применения.
И дело здесь совсем не в непригодности дистиллированной воды для питья. Вредность такой воды из-за отсутствия в ней «полезных» минеральных веществ – это, скорее, укоренившийся предрассудок. Дистиллированная вода действительно имеет невысокие вкусовые качества, часто ее вкус характеризуют как «затхлый». Однако с точки зрения влияния на здоровья нет никаких свидетельств того, что дистиллированная вода непригодна для питья.
Ограниченность же применения дистилляторов в быту объясняется следующими причинами:
Во-первых, бытовые дистилляторы имеют малую производительность (около одного литра в час).
Во-вторых, в бойлере дистиллятора постоянно образуются осадок, накипь и т.п., которые надо вычищать.
В-третьих, дистилляторы излучают тепло и в довольно значительных количествах.
В-четвертых, дистилляторы потребляют значительное количество электроэнергии, что для многих применений делает их использование менее рентабельным, чем обратный осмос (способ очистки воды, при котором вода, проходит через специальную полупроницаемую мембрану) или деминерализация на ионообменных смолах.
Энциклопедия ньюсмейкеров. 2012.
news_enc.academic.ru
Что такое дистилляция, где применяется, описание процесса
Что такое дистилляция? Это процесс, заключающийся в превращении жидкости в пар, который затем снова конденсируется в жидкую форму. Простейшим примером может служить дистилляция воды, когда пар из чайника осаждается в виде капель на холодной поверхности.
Применение и история
Дистилляция используется для отделения жидкостей от нелетучих твердых веществ, как при перегонке спиртных напитков из сброженных материалов, или для разделения двух или более жидкостей с различной температурой кипения, как при производстве бензина, керосина и смазочных масел из нефти. Другие промышленные применения включают переработку таких химических продуктов, как формальдегид и фенол, опреснение морской воды.
Процесс дистилляции, вероятно, использовался еще древними экспериментаторами. Аристотель (384-322 гг. до н. э.) упоминал, что чистую воду можно получить путем испарения морской. Плиний Старший (23-79 гг. н. э.) описал примитивный способ конденсации, при котором масло, получаемое путем нагревания канифоли, собирается на шерсти, помещенной в верхней части перегонного куба.
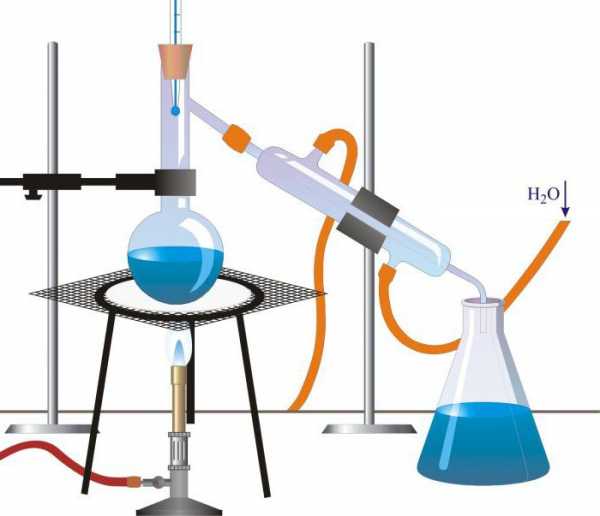
Простая дистилляция
Большинство методов дистилляции, применяемых в промышленности и лабораторных исследованиях, являются вариациями простой перегонки. В этой базовой технологии используется куб или реторта, в которых жидкость нагревается, конденсатор для охлаждения пара и емкость для сбора дистиллята. При нагреве смеси веществ в первую очередь перегоняется наиболее летучее из них или то, у которого температура кипения минимальна, а затем дистиллируются другие, или не дистиллируются совсем. Такой простой аппарат прекрасно подходит для очистки жидкости, содержащей нелетучие компоненты, и достаточно эффективен для разделения веществ с разной точкой кипения. Для лабораторного использования части аппарата обычно делают из стекла и соединяют их пробками, резиновыми шлангами или стеклянными трубками. В промышленных масштабах оборудование делают из металла или керамики.

Фракционная дистилляция
Метод, называемый фракционной, или дифференциальной, дистилляцией, был разработан для нефтепереработки, потому что простая перегонка для разделения жидкостей, температура кипения которых мало отличается, неэффективна. При этом пары многократно конденсируются и испаряются в изолированной вертикальной емкости. Особую роль здесь играют сухопарники, фракционные колонны и конденсаторы, позволяющие вернуть некоторую часть конденсата назад в куб. Цель состоит в том, чтобы добиться тесного контакта между поднимающимися разными фазами смеси, чтобы только самые летучие фракции в форме пара достигали приемника, а остальное возвращалось в виде жидкости в сторону куба. Очищение летучих компонентов в результате контакта между такими противотоками называется ректификацией, или обогащением.
Многократная дистилляция
Данный метод еще называют многостадийным мгновенным испарением. Это еще один вид простой перегонки. С его помощью производится, например, дистилляция воды на крупных коммерческих опреснительных установках. Преобразование жидкости в пар не требует нагрева. Она просто попадает из емкости с высоким атмосферным давлением в емкость с более низким. Это приводит к быстрому испарению, сопровождающемуся конденсацией пара в жидкость.

Вакуумная перегонка
В одной из разновидностей процесса с пониженным давлением для создания вакуума используется вакуумный насос. Этот метод, называемый «вакуумная дистилляция», иногда применяется при работе с веществами, которые обычно кипят при высоких температурах или разлагаются при кипении в нормальных условиях.
Вакуумные насосы создают в колонне давление, которое значительно ниже атмосферного. В дополнение к ним используются вакуумные регуляторы. Тщательный контроль параметров очень важен, поскольку эффективность разделения зависит от различия в относительной летучести при данной температуре и давлении. Изменение этого параметра может негативно повлиять на ход процесса.
Что такое дистилляция в вакууме, хорошо знают на нефтеперерабатывающих заводах. Обычные методы перегонки отделяют легкие углеводороды и примеси от тяжелых углеводородов. Остаточный продукт подвергают вакуумной дистилляции. Это позволяет отделить высококипящие углеводороды, такие как масла и воски, при невысоких температурах. Метод также применяется при разделении чувствительных к нагреву органических химических соединений и для восстановления органических растворителей.
Что такое дистилляция паром?
Паровая перегонка является альтернативным методом перегонки при температурах ниже нормальной точки кипения. Она применяется, когда дистиллируемое вещество не смешивается и химически не реагирует с водой. Примерами таких материалов являются жирные кислоты и соевое масло. В ходе перегонки в жидкость подается пар, который нагревает ее и вызывает испарение.
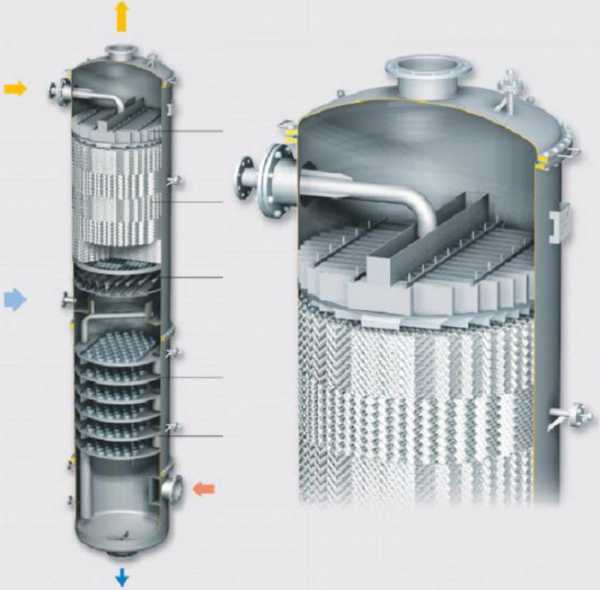
Дистилляция в насадочной колонне
Хотя насадочные колонны чаще всего применяются для абсорбции, они также используются для перегонки парожидкостных смесей. Такая конструкция обеспечивает большую площадь контактной поверхности, что повышает эффективность системы. Другое название такой конструкции – ректификационная колонна.
Принцип работы заключается в следующем. Сырьевая смесь компонентов с разной волатильностью подается в центр колонны. Жидкость стекает вниз через насадку, а пар движется вверх. Смесь в нижней части резервуара попадает в подогреватель и выходит из него вместе с паром. Газ устремляется вверх через насадку, подхватывая наиболее летучие компоненты жидкости, выходит из колонны и попадает в конденсатор. После сжижения продукт поступает в сборник флегмы, где он разделяется на дистиллят и фракцию, используемую для орошения.
Различная концентрация приводит к тому, что менее летучие компоненты переходят из паровой фазы в жидкую. Насадка увеличивает продолжительность и площадь контакта, что повышает эффективность разделения. На выходе пар содержит максимальное количество летучих компонентов, в то время как в жидкости их концентрация минимальна.

Насадки заполняются в навал и пакетами. Форма наполнителя может быть либо случайной, либо геометрически структурированной. Его делают из инертного материала, такого как глина, фарфор, пластик, керамика, металл или графит. Наполнитель, как правило, имеет размеры от 3 до 75 мм и отличается большой площадью поверхности, контактирующей с парожидкостной смесью. Преимущество заполнения в навал заключается в большой пропускной способности, стойкости к большим давлениям и низкой стоимости.
Металлические наполнители имеют высокую прочность и хорошую смачиваемость. Керамические обладают еще более высокой смачиваемостью, но они не такие прочные. Пластиковые достаточно прочны, но плохо смачиваются при низкой скорости потока. Поскольку керамические наполнители устойчивы к коррозии, они используются при повышенных температурах, которые пластик не выдерживает.
Пакетные насадки представляют собой структурированную сетку, размеры которой соответствуют диаметру колонны. Обеспечивают наличие длинных каналов для потоков жидкости и пара. Они дороже, но позволяют снизить перепады давления. Пакетным насадкам отдается предпочтение при невысокой скорости потока и в условиях низкого давления. Обычно их делают из древесины, листового металла или тканой сетки.
Применяются для восстановления растворителей и в нефтехимической промышленности.
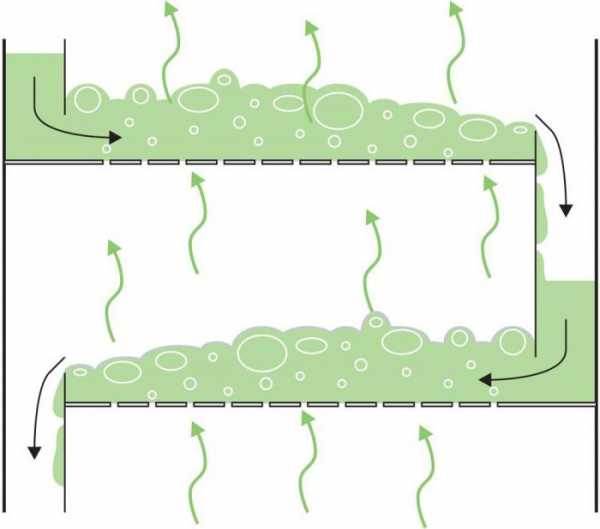
Дистилляция в ректификационной колонне
Наиболее широкое распространение получили колонны тарельчатого типа. Количество тарелок зависит от желаемой чистоты и сложности разделения. Оно влияет на то, какой высоты будет ректификационная колонна.
Принцип работы ее следующий. Смесь подается посредине высоты колонны. Разница в концентрации приводит к тому, что менее летучие компоненты переходят из потока пара в поток жидкости. Газ, выходящий из конденсатора, содержит наиболее летучие вещества, а менее испаряемые выходят через нагреватель в поток жидкости.
Геометрия тарелок в колонне влияет на степень и тип контакта между разными фазовыми состояниями смеси. Конструктивно они выполняются ситчатыми, клапанными, колпачковыми, решетчатыми, каскадными и т. д. Ситчатые тарелки, в которых имеются отверстия для пара, используются для обеспечения высокой производительности при низких затратах. Более дешевые клапанные тарелки, в которых отверстия снабжены открывающими и закрывающими клапанами, склонны к засорению из-за скопления на них материала. Колпачковые снабжены колпачками, позволяющими пару проходить через жидкость сквозь крошечные отверстия. Это самая передовая и дорогая технология, эффективная при низких скоростях потока. Жидкость течет от одной тарелки к другой вниз по сливным вертикальным трубам.
Тарельчатые колонны часто используются для восстановления растворителей из технологических отходов. Также они применяются для восстановления метанола при операции сушки. В качестве жидкого продукта выходит вода, а летучие органические отходы переходят в паровую фазу. Вот что такое дистилляция в ректификационной колонне.

Криогенная перегонка
Криогенная дистилляция заключается в применении общих методов перегонки к газам, охлажденным до жидкого состояния. Система функционирует при температурах ниже -150 °С. Для этого используются теплообменники и змеевики. Вся конструкция называется криогенным блоком. Сжиженные газы поступают в блок и перегоняются при очень низких температурах. Колонны криогенной дистилляции могут быть насадочными и пакетными. Пакетный дизайн более предпочтителен, поскольку насыпной материал менее эффективен при низких температурах.
Одним из основных применений криогенной дистилляции является разделение воздуха на составляющие его газы.
Экстрактивная перегонка
В экстрактивной ректификации используются дополнительные соединения, которые действуют как растворитель для изменения относительной летучести одного из компонентов смеси. В экстрактивную колонну к разделяемым веществам добавляется растворитель. Компонент сырьевого потока, который требуется извлечь, соединяется с растворителем и выходит в жидкой фазе. Другой компонент испаряется и выходит в дистиллят. Вторая перегонка в другой колонне позволяет отделить вещество от растворителя, который затем возвращается на предыдущий этап, чтобы повторить цикл.
Экстрактивная ректификация применяется для разделения соединений с близкими температурами кипения и азеотропных смесей. Экстрактивная ректификация не так широко распространена в промышленности, как обычная дистилляция, из-за сложности конструкции. Примером является процесс получения целлюлозы. Органический растворитель отделяет целлюлозу от лигнина, а вторая перегонка позволяет получить чистое вещество.
fb.ru
Дистилляция. Справка — РИА Новости, 11.12.2009
Определенная роль в совершенствовании процесса дистилляции принадлежит алхимикам средневековья, но наибольшее развитие она получила в конце 19 – начале 20 веков в связи с внедрением в промышленности (спиртовой, нефтеперерабатывающей и др.) высокопроизводительных колонных аппаратов.
В зависимости от физических свойств компонентов разделяемых жидких смесей применяют различные способы дистилляции.
Простая дистилляция проводится частичным испарением кипящей жидкой смеси, непрерывным отводом и последующей конденсацией образовавшихся паров. Так как пары над кипящей жидкой смесью содержат низкокипящих компонентов больше, чем жидкость, то конденсат (называемый дистиллятом) обогащается, а неиспарившаяся жидкость (кубовый остаток) обедняется ими. При простой дистилляции содержание низкокипящих компонентов в паровой и жидкой фазах непрерывно падает. Поэтому состав дистиллята меняется во времени. Простая дистилляция – периодический процесс. Для ускорения процесса применяют полунепрерывную дистилляцию, при которой в дистилляционный куб непрерывно поступает исходная смесь, равная массе уходящих паров.
Фракционная дистилляция, называемая также дробной перегонкой, – одна из разновидностей простой дистилляции. Такую дистилляцию применяют для разделения смеси жидкостей на фракции, кипящие в узких интервалах температур. При этом дистилляты разных составов отводят (последовательно во времени) в несколько сборников. В каждом из этих дистиллятов (фракциях) преобладает один или несколько компонентов исходной смеси с близкими температурами кипения. Простую дистилляцию для улучшения разделения смесей часто комбинируют с противоточной дефлегмацией (частичная конденсация). При этом образующиеся в кубе пары частично конденсируются в дефлегматоре, конденсат (флегма) непрерывно возвращается в куб, а остаток паров после дефлегматора поступает в конденсатор, откуда дистиллят стекает в сборник. Этим способом достигается большее обогащение дистиллята низкокипящими компонентами, т.к. при дефлегмации паров преимущественно конденсируются высококипящие компоненты.
Равновесная дистилляция (однократное испарение) характеризуется испарением части жидкости и продолжительным контактом паров с неиспарившейся жидкостью до достижения фазового равновесия. Разделяемая смесь проходит по трубам, обогреваемым снаружи топочными газами. Образовавшаяся при этом парожидкостная смесь, близкая к равновесному состоянию, поступает в сепаратор для механического отделения жидкости от пара. Пары из сепаратора поступают в конденсатор, откуда дистиллят стекает в приемник, а оставшаяся в сепараторе жидкость отводится в сборник. В этом процессе соотношение между паром и жидкостью определяется материальным балансом и условиями фазового равновесия. Равновесная дистилляция редко применяется для двухкомпонентных смесей; хорошие результаты получают в основном в случае многокомпонентных смесей, из которых можно получить фракции, сильно различающиеся по составу.
Дистилляцию в токе водяного пара или инертных газов применяют, когда необходимо понизить температуру процесса отгонки, в случае разделения нетермостойких компонентов, а также для отгонки веществ с низкой температурой испарения от компонентов с высокой температурой испарения. Пузырьки водяного пара или инертного газа барботируют (продавливают) через слой жидкости. При дистилляции с водяным паром образовавшаяся смесь паров воды и летучего компонента отводится из аппарата и подвергается конденсации и охлаждению. Состав образующихся в кубе паров не зависит от состава жидкости, а температура кипения смеси всегда ниже температуры кипения каждого из компонентов при данном давлении. При дистилляции с инертным газом компоненты раствора испаряются в поток газа, даже если раствор не кипит, а парообразование при испарении может происходить при любых температурах, вне зависимости от внешнего давления, что позволяет вести процесс при низких температурах.
Молекулярная дистилляция основана на разделении жидких смесей свободным их испарением в высоком вакууме 133–13,3 мн/м2 (10–3–10–4 мм ртутного столба) при температуре ниже точки их кипения. Процесс проводят при взаимном расположении поверхностей испарения и конденсации на расстоянии, меньшем длины свободного пробега молекул перегоняемого вещества. Благодаря вакууму молекулы пара движутся от испаряющей поверхности к конденсирующей с минимальным числом столкновений. При молекулярной дистилляции изменение состава пара по сравнению с составом жидкости определяется различием скоростей испарения компонентов. Поэтому этим способом можно разделять смеси, компоненты которых обладают одинаковым давлением паров. При данной температуре жидкости и соответствующем ей давлении паров скорость молекулярной дистилляции растет с понижением давления в аппарате.
Для молекулярной дистилляции применяют аппараты с горизонтальными и вертикальными поверхностями испарения, а также получившие наибольшее промышленное применение центробежные аппараты. В последних процесс характеризуется наименьшими толщиной жидкой пленки (в среднем 0,05 мм) и временем ее пребывания на поверхности нагрева (0,03м–1,2 сек). В центробежных аппаратах на испаритель, представляющий собой быстровращающийся конус (иногда диск), подается разделяемая смесь. Центробежная сила перемещает жидкость от центра к периферии (вверх). Пары перегоняемого вещества собираются на неподвижном конденсаторе, расположенном параллельно поверхности испарителя, откуда дистиллят непрерывно отводится. Остаток после перегонки сбрасывается в кольцевой желоб и выводится из куба. Для увеличения эффекта разделения устанавливают несколько аппаратов последовательно.
Молекулярную дистилляцию применяют для разделения и очистки высокомолекулярных и термически нестойких органических веществ, например для очистки эфиров себациновой, стеариновой, олеиновой и других кислот, для выделения витаминов из рыбьего жира и различных растительных масел, при производстве медицинских препаратов, вакуумных масел и др.
В металлургии понятие дистилляции объединяет пирометаллургические процессы, основанные на переводе восстанавливаемого металла в парообразное состояние с последующей конденсацией. Металлургическая дистилляция – сочетание химического (окислительно-восстановительной реакции) и физического (испарения и конденсации) процессов. Восстановление проводят с использованием углеродистых восстановителей или металлотермическим способом. Возможно выделение свободного металла при окислительном обжиге сульфидных концентратов. Степень разделения при дистилляции определяется различием состава перегоняемой смеси и ее пара. Полнота перехода металла в газовую фазу при дистилляции определяется восстановлением металлов при температурах и давлениях, обеспечивающих получение восстановленного металла в парообразном агрегатном состоянии.
Дистилляция применяется также в химической, лесохимической, фармацевтической и других отраслях промышленности для грубого разделения смесей на фракции, когда не предъявляются высокие требования к чистоте получаемых продуктов, а также для очистки жидких смесей от нелетучих или малолетучих примесей.
Дистилляцию с дефлегмацией применяют в нефтепереработке и лабораторной практике, дистилляция с водяным паром – в химической, нефтехимической, парфюмерной и других отраслях промышленности для отгонки высококипящих компонентов из вязких смесей, содержащих значительные количества твердых или малолетучих жидких веществ. Также путем перегонки (однократной или многократной) на ликеро-водочных заводах получают полуфабрикат для множества алкогольных напитков: коньяка, рома, виски, а в домашних условиях – самогон.
В лабораторной практике условия дистилляции для некоторых видов продуктов стандартизованы. Наиболее известными являются ГОСТ 2177(ASTM D86) – перегонка 100 мл продукта с температурой кипения от комнатной до 400°С при атмосферном давлении. Это сделано для воспроизводимости результатов тестирования бензина, керосина, дизельного топлива, нефти, а также различных растворителей.
Дистилляция является давно известным и проверенным способом глубокой очистки воды.
Хорошо всем известный пример использования дистиллированной воды – заливка в аккумуляторы автомобиля. В быту же дистилляторы не нашли широкого применения.
И дело здесь совсем не в непригодности дистиллированной воды для питья. Вредность такой воды из-за отсутствия в ней «полезных» минеральных веществ – это, скорее, укоренившийся предрассудок. Дистиллированная вода действительно имеет невысокие вкусовые качества, часто ее вкус характеризуют как «затхлый». Однако с точки зрения влияния на здоровья нет никаких свидетельств того, что дистиллированная вода непригодна для питья.
Ограниченность же применения дистилляторов в быту объясняется следующими причинами:
Во-первых, бытовые дистилляторы имеют малую производительность (около одного литра в час).
Во-вторых, в бойлере дистиллятора постоянно образуются осадок, накипь и т.п., которые надо вычищать.
В-третьих, дистилляторы излучают тепло и в довольно значительных количествах.
В-четвертых, дистилляторы потребляют значительное количество электроэнергии, что для многих применений делает их использование менее рентабельным, чем обратный осмос (способ очистки воды, при котором вода, проходит через специальную полупроницаемую мембрану) или деминерализация на ионообменных смолах.
ria.ru
